
24 июня 2015
В неожиданном открытии Институт Солка и его сотрудники показали, как отключение защиты теломер во время клеточного деления вызывает гибель клеток.
В неожиданном открытии Институт Солка и его сотрудники показали, как отключение защиты теломер во время клеточного деления вызывает гибель клеток.
LA JOLLA-теломеры, специализированные концы наших хромосом, которые определяют, как долго клетки могут продолжать воспроизводить себя, давно изучались на предмет их связи с процессом старения и Онкология. Теперь открытие в Институте Солка показывает, что теломеры могут играть более важную роль, чем считалось ранее, в программе самоуничтожения в клетках, которая предотвращает опухоли, функция, которая потенциально может быть использована для улучшения лечения рака.
Когда клетки размножаются в процессе, называемом митозом, их теломеры каждый раз становятся немного короче. В конце концов, после многих клеточных делений теломеры становятся критически короткими, сигнализируя клетке о прекращении деления. Этот нормальный процесс действует как барьер против рака. Однако клетки, у которых есть дефекты в сигнальном пути, продолжают саморазрушаться и после этой стадии.
Этот процесс разрушения клеток, называемый кризисом, обычно препятствует репликации генетически нестабильных или поврежденных клеток. Но многие типы раковых клеток обходят кризис, защищая теломеры, чтобы препятствовать сигналу самоуничтожения и позволяя клеткам продолжать размножаться.
«Мы задались целью понять механизм гибели клеток при кризисе и обнаружили гораздо более активную роль теломер в качестве барьеров для развития опухоли, чем считалось ранее», — говорится в сообщении. Ян Карлседер, профессор Солк в Лаборатория молекулярной и клеточной биологии и старший автор работы. «Это началось, когда мы увидели, что митоз длится дольше в клетках, приближающихся к кризису». Работа была подробно описана в Природа июня 24, 2015.
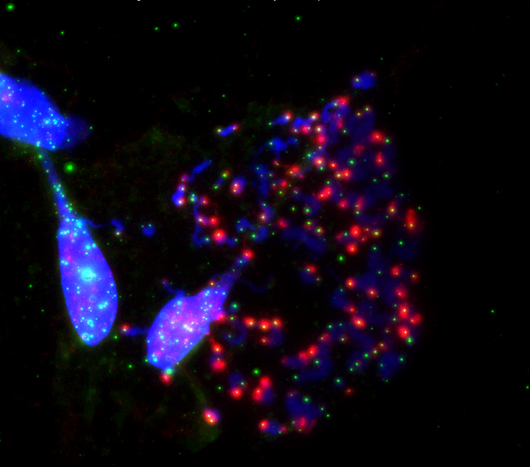
Исследователи Солка показывают, как нарушение защиты концов хромосом (синие), называемых теломерами (зеленые), во время клеточного деления (митоза) вызывает гибель клеток. Это происходит, когда белок, защищающий теломеры, TRF2, ингибируется. На этом изображении показано обострение снятия защиты с теломер (красный цвет) во время остановки митоза путем искусственного манипулирования TRF2.
Открыть для изображения с высоким разрешением.
Изображение: предоставлено Институтом биологических исследований Солка.
В то время как регулярный митоз обычно длится около 30-45 минут, клетки, которые вот-вот вступят в кризис, имеют митоз, который длится 2-20 часов или более. Наблюдение за этим напомнило исследователям 2012 discovery где искусственно удлиняли процесс митоза. Как правило, теломеры имеют белок, защищающий их от идентификации клеткой как поврежденной ДНК и, таким образом, предотвращающий их гибель. Но во время искусственно удлиненного митоза теломеры теряли белок, вызывая сигнал о повреждении ДНК, который подталкивал клетки к самоуничтожению.
К своему удивлению, ученые обнаружили, что точно то же самое происходит и в состоянии естественного кризиса. В этой новой работе исследователи в режиме реального времени визуализировали клетки в чашке, чтобы отслеживать судьбу клеток в течение одного или нескольких митотических циклов. Они обнаружили, что тип клеточного стресса, называемый слиянием теломер, может вызвать длительный митоз и, в конечном итоге, кризис. Клетки в этом состоянии теряли белок, защищающий теломеры, и активировали последовательность самоуничтожения.
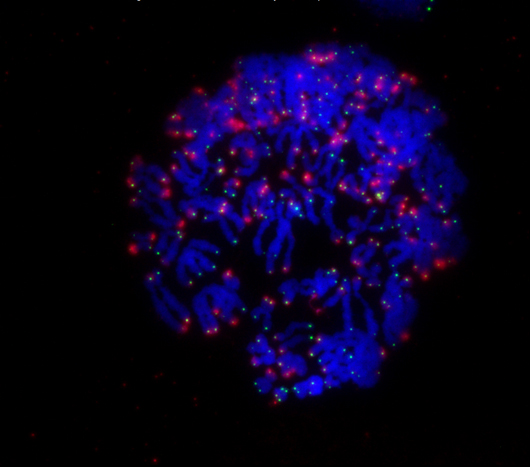
Во время митоза хромосомы клетки (синие) быстро делятся. Когда концы хромосом, называемые теломерами (зеленые), больше не защищены белком TRF2, клетка получает сигнал (красный) о гибели клетки.
Открыть для изображения с высоким разрешением.
Изображение: предоставлено Институтом биологических исследований Солка.
«Существовала давняя гипотеза, которая оказалась неверной: клетки просто начинают сливать хромосомы и распадаться, вызывая нестабильность и гибель клеток», — говорит Карлседер, который также является заведующим кафедрой Дональда и Дарлин Шили Солка. «Вместо этого мы показываем, что это гораздо более целенаправленный путь, которому действительно требуется всего один клеточный цикл, чтобы вызвать кризис — он не имеет ничего общего с медленным и постоянным накоплением геномной нестабильности».
Энтони Чезаре, глава группы проверки целостности генома в Детский медицинский научно-исследовательский институт в Австралии и участник работы, сказал, что открытие было очень захватывающим и что было неожиданно увидеть, как события раннего клеточного цикла, слияния теломер, передаются на более позднюю стадию клеточного цикла, митоз. «Это открывает новые возможности для понимания того, как теломеры контролируют рост клеток, и значения биологии теломер в химиотерапии», — говорит он.
Некоторые химиотерапевтические препараты, такие как таксол для лечения рака молочной железы, направлены на остановку рака путем прерывания митоза, чтобы раковые клетки больше не могли делиться. Исследователи предполагают, что они могут усиливать эти митотические ингибиторы, например, снимая защиту с теломер, чтобы сделать клетки более восприимчивыми к лекарствам. Также можно было бы увидеть, имеют ли клетки из конкретной опухоли более короткие или незащищенные теломеры, и, если это так, ожидать, что эта опухоль будет гораздо более чувствительна к митотическим ингибиторам.
«Обнаруженный нами путь ставит под сомнение давнюю гипотезу о клеточном поведении во время раннего образования опухоли», — говорит Макото Хаяси, исследователь Центра перспективных исследований Хакуби Киотского университета и первый автор новой работы. «Всестороннее понимание пути, как мы надеемся, предоставит нам новый метод ранней диагностики опухолей и терапевтические возможности для очень ранних стадий рака».
В настоящее время лаборатория работает с Деборой Кадо, доктором медицины и магистром наук, в Калифорнийском университете в Сан-Диего, чтобы проверить эти теории на пациентах с недавно диагностированным раком молочной железы.
Авторами исследования являются Макото Т. Хаяши из Киотского университета, Энтони Дж. Чезаре из Детского медицинского исследовательского института, а также Тереза Ривера и Ян Карлседер из Института Солка.
Эта работа финансировалась Программа Human Frontier Science и Японское общество поощрения научных стипендий для постдокторских исследований за рубежом, Национальные институты здоровья, кресло Дональда и Дарлин Шили, Фонд Хайленд-стрит, Фонд Фрица Б. Бернса, Изумрудный фонд, и Центр исследований старения Гленна.
ЖУРНАЛ
Природа
АВТОРЫ
Макото Т. Хаяши, Энтони Дж. Чезаре, Тереза Ривера и Ян Карлседер
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.