
7 июня 2021
Исследование Солка показывает, как оптимизировать производство клеток, продуцирующих инсулин, из стволовых клеток.
Исследование Солка показывает, как оптимизировать производство клеток, продуцирующих инсулин, из стволовых клеток.
LA JOLLA — Диабет 1 типа, который возникает, когда поджелудочная железа не вырабатывает достаточное количество инсулина для контроля уровня глюкозы в крови, представляет собой заболевание, которое в настоящее время неизлечимо и с которым большинству пациентов трудно справиться. Ученые из Института Солка разрабатывают многообещающий подход к его лечению: использование стволовых клеток для создания клеток, продуцирующих инсулин (называемых бета-клетками), которые могли бы заменить нефункционирующие клетки поджелудочной железы.
В исследовании, опубликованном 7 июня 2021 года в журнале Природа связиИсследователи сообщили, что они разработали новый способ создания бета-клеток, который намного эффективнее, чем предыдущие методы. Кроме того, когда эти бета-клетки были протестированы на мышиной модели диабета 1 типа, уровень сахара в крови животных был взят под контроль в течение примерно двух недель.
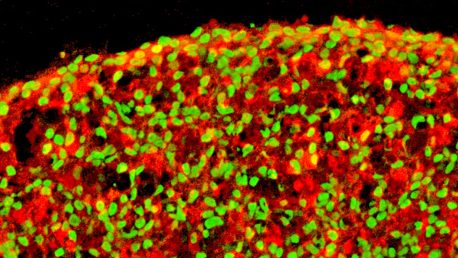
Открыть для изображения с высоким разрешением.
«Стволовые клетки — чрезвычайно многообещающий подход для разработки многих клеточных методов лечения, в том числе более эффективных методов лечения диабета 1 типа», — говорит профессор Солк. Хуан Карлос Исписуа Бельмонте, старший автор статьи. «Этот метод производства большого количества безопасных и функциональных бета-клеток является важным шагом вперед».
В текущей работе исследователи начали с человеческих плюрипотентных стволовых клеток (чПСК). Эти клетки, которые могут быть получены из тканей взрослого человека (чаще всего из кожи), потенциально могут стать клетками любого типа, обнаруженными во взрослом организме. Используя различные факторы роста и химические вещества, исследователи постепенно превращали hPSCs в бета-клетки, что имитировало развитие поджелудочной железы.
Производство бета-клеток из hPSC в лаборатории не ново, но в прошлом выход этих драгоценных клеток был низким. С помощью существующих методов только от 10 до 40 процентов клеток становятся бета-клетками. Для сравнения, методы, используемые для создания нервных клеток из hPSC, имеют выход около 80 процентов. Другая проблема заключается в том, что если в смеси останутся недифференцированные клетки, они могут в конечном итоге превратиться в другую клетку, которая будет нежелательной.
«Чтобы лечение на основе бета-клеток в конечном итоге стало жизнеспособным вариантом для пациентов, важно упростить производство этих клеток», — говорит соавтор Хайсон Лю, бывший сотрудник лаборатории Бельмонте. «Нам нужно найти способ оптимизировать процесс».
Чтобы решить эту проблему, исследователи применили поэтапный подход к созданию бета-клеток. Они идентифицировали несколько химических веществ, которые важны для индукции превращения hPSCs в более специализированные клетки. В конечном итоге они определили несколько коктейлей химических веществ, которые привели к выходу бета-клеток до 80 процентов.
Они также изучили способы выращивания этих клеток в лаборатории. «Обычно клетки выращивают на плоской пластине, но мы позволили им расти в трех измерениях», — говорит соавтор Ронгуи Ли, научный сотрудник лаборатории Бельмонте. Выращивание клеток таким образом создает большую общую площадь поверхности между клетками и позволяет им влиять друг на друга, как это было бы во время развития человека.
После того, как клетки были созданы, их трансплантировали мышиной модели диабета 1 типа. У модельных мышей была модифицированная иммунная система, которая не отторгала трансплантированные клетки человека. «Мы обнаружили, что в течение двух недель у этих мышей уровень сахара в крови снизился до нормального уровня», — говорит соавтор Синь-Кай Ляо, научный сотрудник лаборатории Бельмонте. «Трансплантированные бета-клетки, полученные из чПСК, оказались биологически функциональными».
Исследователи продолжат изучать этот метод в лаборатории для дальнейшей оптимизации производства бета-клеток. Необходимы дополнительные исследования для оценки вопросов безопасности, прежде чем можно будет начать клинические испытания на людях. Исследователи говорят, что методы, описанные в этой статье, также могут быть полезны для разработки специализированных клеток для лечения других заболеваний.
Среди других авторов были Чао Ван, Ян Юй, Лэй Ши и Цзямэн Дан из Солка; Чжэинг Минь из Пекинского университета; Альберто Хайек из Калифорнийского университета в Сан-Диего; и Льянос Мартинес Мартинес и Эстрелла Нуньес Деликадо из Католического университета Сан-Антонио-де-Мурсия в Испании.
Эта работа финансировалась Католическим университетом Сан-Антонио-де-Мурсия, Primafrio, Фондом Ларри Л. Хиллблома, Фондом Мокси и Diabetes Research Connection (номер проекта: 15; номер проекта учреждения: Liu-DRC-2019).
ЖУРНАЛ
Природа связи
АВТОРЫ
Лю Хайсон, Ронхуэй Ли, Синь-Кай Ляо, Чжэин Минь, Чао Ван, Ян Юй, Лэй Ши, Цзямэн Дан, Альберто Хайек, Льянос Мартинес Мартинес, Эстрелла Нуньес Деликадо, Хуан Карлос Исписуа Бельмонте
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.