
3 декабря 2008
Ла-Хойя, Калифорния. Долгое время считавшиеся простыми сторонними наблюдателями, астроциты имеют решающее значение для выживания и благополучия двигательных нейронов, которые контролируют произвольные движения мышц. На самом деле, дефектные астроциты могут опустошать двигательные нейроны и являются главными подозреваемыми в атрофическом амиотрофическом боковом склерозе (БАС).
Чтобы добраться до корня этих сложных отношений, исследователи из Института биологических исследований Солка впервые создали систему на основе эмбриональных стволовых клеток человека (hESC) для моделирования БАС. Их исследование подтвердило, что дисфункциональные астроциты человека выступают против своих зарядов и убивают здоровые двигательные нейроны. Но что еще более важно, обработка культивируемых клеток апоцинином, мощным антиоксидантом, предотвращала гибель двигательных нейронов, вызванную неисправностью астроцитов.
Их выводы, опубликованные в номере журнала от 4 декабря. Сотовые стволовых клеток, дают новое представление о токсических путях, которые способствуют гибели двигательных нейронов при БАС, и открывают новые возможности для экспериментов по скринингу наркотиков с использованием человеческого БАС. в пробирке моделей, а также клинических вмешательств с использованием клеточной терапии на основе астроцитов.
«Множество препаратов, продемонстрировавших значительную эффективность на моделях на мышах, не сдержали своих обещаний как в доклинических, так и в клинических испытаниях», — говорит Фред Х. Гейдж, кандидат биологических наук, профессор лаборатории генетики, руководивший исследованием. На самом деле только одно лекарство — рилузол — было одобрено FDA для лечения БАС, и оно замедляет течение болезни всего на два месяца.
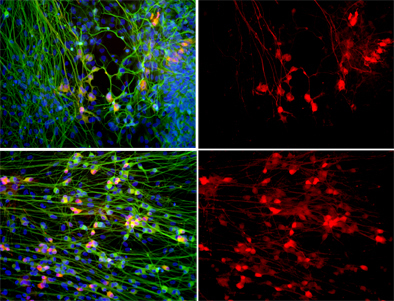
Вверху: Когда мотонейроны (показаны красным) выращиваются в присутствии дефектных астроцитов, их количество резко падает. Внизу: обработка культур апоцинином, мощным антиоксидантом, значительно увеличивает выживаемость мотонейронов. Ядра всех клеток отмечены синим цветом, а нейроны показаны зеленым. Правая панель: показаны только мотонейроны.
Изображение: предоставлено доктором М. Кэрол Маркетто, Институт биологических исследований Солка.
«Существует острая потребность в новых моделях БАС, которые потенциально можно будет применить в клинических испытаниях и которые можно будет, как минимум, использовать в сочетании с моделями на мышах для проверки лекарств и целей лекарств», — говорит Гейдж.
БАС, также известный как болезнь Лу Герига, был назван в честь легендарного отбивающего игрока команды «Нью-Йорк Янкиз», который дал свое имя загадочной болезни более 60 лет назад. Нейродегенеративное заболевание, обычно смертельное, поражает двигательные нейроны, контролирующие произвольные движения, что приводит к прогрессирующему параличу и мышечной атрофии.
Хотя БАС впервые был классифицирован как болезнь более 140 лет назад, до сих пор мало сведений о его причине. Важный шаг к пониманию болезни был сделан, когда ученые обнаружили, что БАС может быть вызван наследственными мутациями в гене, кодирующем фермент SOD1, сокращение от супероксиддисмутазы 1. Этот фермент защищает организм от повреждений, вызванных свободными радикалами, высокореактивными молекулами, продуцируемыми клеток при нормальном обмене веществ.
Моторные нейроны спинного мозга экспрессируют высокие уровни SOD1, что, как многие изначально думали, может объяснить их селективную уязвимость. Но вскоре эксперименты на мышах показали, что дегенерация мотонейронов не обязательно связана с экспрессией дефектного SOD1 в мотонейронах. сам по себе а скорее с его экспрессией в критическом количестве соседних опорных клеток.
Поскольку большинство методов лечения, которые работали на моделях мышей с БАС, не оправдали ожиданий в доклинических и клинических испытаниях, постдокторант и первый автор М. Кэрол Маркетто, доктор философии, искала альтернативу: «Трансгенные мыши, содержащие мутированные человеческие формы SOD1 были очень полезны для изучения возникновения и прогрессирования заболевания. Но мы чувствовали, что модели клеточных культур, использующие как человеческие нейроны, так и астроциты, потенциально могут быть очень полезны для скрининга лекарств и, в некоторой степени, клеточно-заместительной терапии».
Чтобы раскрыть вклад астроцитов в дегенерацию двигательных нейронов человека, Маркетто сначала убедил чЭСК дифференцироваться в двигательные нейроны посредством серии физических манипуляций и воздействия ряда факторов роста. Когда она совместно культивировала эти клетки с человеческими астроцитами, экспрессирующими мутированную форму SOD1, количество живых мотонейронов в чашке Петри резко упало. «При наличии мутации астроциты активировали воспалительную реакцию и начали вырабатывать активные формы кислорода, что является признаком БАС», — говорит Маркетто.
Когда она обработала эти клетки известными антиоксидантами, такими как апоцинин, который содержится во многих растениях, эпикатехин, один из полезных ингредиентов зеленого чая и шоколада, или альфа-липоевая кислота, которая вырабатывается организмом, процент взбивания астроцитов увеличился. количество вредных активных форм кислорода значительно уменьшилось. Мало того, когда она лечила моторные нейроны, культивированные в присутствии мутантных астроцитов, апоцинин — единственный протестированный в эксперименте по совместному культивированию — помог моторным нейронам противостоять их более не поддерживающей среде.
«Мы считаем, что можем использовать эту систему в качестве быстрого скринингового теста на окислительное повреждение лекарств, чтобы выявить лучших кандидатов для последующих долгосрочных экспериментов по совместному культивированию», — говорит Маркетто.
В то время как исследования эффектов мутации гена SOD1 дают важные сведения о возможных причинах гибели двигательных нейронов, на самом деле лишь небольшая часть всех случаев БАС связана с мутацией; явно существуют и другие, пока еще не выявленные генетические причины.
«Быстрый прогресс в технологии индуцированных плюрипотентных стволовых клеток вскоре позволит нам создавать стволовые клетки, специфичные для пациента, которые можно будет использовать в нашем совместном культуральном анализе, чтобы получить новое представление о различных причинах БАС», — говорит Гейдж.
Для получения информации о коммерциализации этой технологии, пожалуйста, свяжитесь с Майком Уайтом по телефону 858-453-4100, x 1703 (mwhite@salk.edu) в Отделе управления и развития технологий Солка.
Это исследование финансировалось Project ALS, Фондом Даны и Кристофера Рив, Калифорнийским институтом регенеративной медицины, Lookout Fund и Национальным институтом здравоохранения.
В число исследователей, которые также внесли свой вклад в работу, входят исследователи с докторской степенью Алиссон Р. Муотри, доктор философии, и Янлинг Му, доктор философии, в лаборатории Гейджа, научный сотрудник с докторской степенью Алан М. Смит, доктор философии, и доцент Габриэла. Г. Сезар, доктор философии, оба в Университете Висконсин-Мэдисон, Мэдисон.
Управление связи
Тел: (858) 453-4100
press@salk.edu