
30 ноября 2016
Новый метод визуализации позволяет исследовать молекулярные смеси
Новый метод визуализации позволяет исследовать молекулярные смеси
Открыть для изображения с высоким разрешением
Предоставлено: Институт Солка.
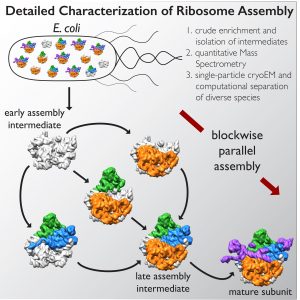
ЛА ХОЛЛА — Рибосомы — макромолекулярные машины, состоящие из РНК и белков, которые скручиваются, складываются и поворачиваются — отвечают за производство всех белков в клетке и могут дать ключ к расшифровке целого ряда заболеваний. Несмотря на сложность рибосом, клетки способны производить до 100,000 XNUMX рибосом каждый час. Но из-за того, что они собираются так быстро, исследователи не смогли понять, как они собираются вместе.
Сотрудничество, возглавляемое Институтом биологических исследований Солка и Исследовательским институтом Скриппса в Ла-Хойя, Калифорния, развернуло передовой метод визуализации, называемый одночастичной криоэлектронной микроскопией (крио-ЭМ), и сопутствующие инструменты анализа для расшифровки некоторых ключевые шаги сборки рибосом, первый шаг к пониманию их роли в здоровье и болезни. Результаты опубликованы онлайн 1 декабря 2016 г. в журнале Ячейка.
«Эти новые структуры, которые мы зафиксировали с помощью крио-ЭМ, показывают, что можно визуализировать и интерпретировать различные молекулярные механизмы в действии», — говорит соавтор исследования. Дмитрий Люмкис, научный сотрудник Helmsley-Salk в Salk. «Это совершенно другой способ видеть и заниматься структурной биологией. Эта статья — яркий пример того, что мы можем проводить гораздо более сложный анализ, чем когда-либо ожидали».
Понимание молекулярных структур важно не только для фундаментальных исследований в области биологии, но и для процесса разработки лекарств, чтобы лучше понять, как делать более безопасные и эффективные лекарства. Исследователи традиционно обращаются к рентгеновской кристаллографии — методу, который требует от пользователей тщательной очистки молекулы, а затем преобразования ее в кристаллическую форму, но у этого метода есть ограничения.

Открыть для изображения с высоким разрешением
Предоставлено: Институт Солка.
За последние несколько лет достижения в области крио-ЭМ позволили ученым получать изображения отдельных частиц с разрешением, сравнимым с разрешением традиционных рентгеновских методов. Но в крио-ЭМ с одной частицей белки («частицы») мгновенно замораживаются и визуализируются с использованием потоков электронов, что означает, что молекулы не нужно кристаллизовать, и они могут сохранить большую часть своей естественной структуры. Хотя крио-ЭМ существует уже некоторое время, новые камеры упрощают захват белков с высоким разрешением до того, как их поразит электронный спрей.
Важно отметить, что вычислительные инструменты для анализа данных крио-ЭМ достигли такого совершенства, что теперь исследователи могут очищать молекулы. в кремнеземе с помощью компьютера, а не с помощью традиционных биохимических подходов. Это становится гораздо более мощным подходом к разделению смесей видов, позволяя исследователям идентифицировать и различать структурно различные популяции частиц более подробно, чем раньше.
В новом исследовании старший соавтор Джеймс Уильямсон, профессор молекулярной биологии и химии в Исследовательском институте Скриппса, и его команда разработали метод, позволяющий предотвратить столь быстрое объединение одного из основных компонентов рибосом, 50-й субъединицы. Ученые смогли химически приостановить смесь различных молекул на разных стадиях сборки.
Затем группа Люмкиса использовала крио-ЭМ высокого класса для изображения и анализа этих застопорившихся структур, что не было предпринято для такого сочетания разнообразных форм конкретной молекулы.
«Другие показали, что вы можете зафиксировать пару различных структурных состояний молекулы», — говорит Люмкис. «Но, насколько я знаю, никто не пытался взять эту грубую смесь вещей, поместить ее на сетку крио-ЭМ и спросить, что там было».
Открыть для изображения с высоким разрешением
Предоставлено: Институт Солка.
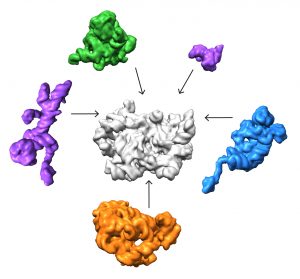
Команда обнаружила, что в смеси есть по крайней мере 15 типов комплексов, 13 из которых активно собирают 50-е субъединицы. Они визуализировали каждую из этих структур с разрешением, достаточно высоким, чтобы расшифровать составляющие белка и РНК. Затем они смогли использовать компьютерные алгоритмы для упорядочения комплексов в соответствии с их путем сборки.
По словам Уильямсона, анализ группы предполагает, что рибосомы могут собираться несколькими разными путями, что важно для обеспечения эффективности процесса и способности противостоять различным клеточным стрессам. «Если представить сборочную линию, где каждый шаг должен выполняться в последовательном порядке, и на одном из этих шагов возникает проблема, все останавливается», — говорит он. «Если есть параллельные пути, то сборка может идти по другим каналам, пока проблема не будет решена.
Ученым потребовалось больше года, чтобы разобраться в структурах, используя относительно новые инструменты анализа изображений. Но они заложили основу для изучения других больших, динамичных и структурно гетерогенных молекулярных машин, которые, по словам Люмкиса, приведут к новым фундаментальным научным и трансляционным открытиям.
Другими авторами исследования являются Джозеф Х. Дэвис из Научно-исследовательский институт Скриппса; и Юн Цзи Тан, Бриджит Каррагер и Клинтон Поттер из Колумбийский университет и Нью-Йоркский центр структурной биологии.
Исследование было поддержано Фонд Джейн Коффин Чайлд; Национальный институт старения; Благотворительный фонд Леоны М. и Гарри Б. Хелмсли; Национальный институт общих медицинских наук; Фонд Симонс; и Агентство науки, технологий и исследований Сингапура.
ЖУРНАЛ
Ячейка
АВТОРЫ
Джозеф Х. Дэвис, Йонг Зи Тан, Бриджит Каррагер, Клинтон С. Поттер, Дмитрий Люмкис, Джеймс Р. Уильямсон
Управление связи
Тел: (858) 453-4100
press@salk.edu
Институт Салка — это независимый некоммерческий исследовательский институт, основанный в 1960 году Джонасом Салком, разработчиком первой безопасной и эффективной вакцины против полиомиелита. Миссия Института — проводить фундаментальные, совместные, рискованные исследования, направленные на решение наиболее актуальных проблем общества, включая рак, болезнь Альцгеймера и уязвимость сельского хозяйства. Эта фундаментальная наука лежит в основе всех усилий по внедрению результатов исследований в практику, генерируя знания, которые позволяют создавать новые лекарства и инновации во всем мире.