
2009 년 8 월 9 일
LA JOLLA, CA - Salk Institute for Biological Studies 연구원들의 공동 연구에서 "게놈의 수호자"라는 이름을 얻은 종양 억제 인자 p53이 암이 될 수 있는 세포를 멈출 뿐만 아니라 체세포 리프로그래밍.
과학자들이 피부 세포와 같은 성인 인간 세포를 소위 유도 만능 줄기 세포(iPSC)로 재프로그래밍하는 방법을 배웠지만 재프로그래밍 효율은 여전히 매우 낮습니다. The Salk 연구, 9월 XNUMX일 사전 온라인 판에 발표 자연, 많은 세포 중 소수의 세포만이 시계를 되돌리도록 설득할 수 있는 이유에 대한 새로운 통찰력을 제공합니다.

Juan-Carlos Izpisúa Belmonte 박사와 Geoffrey M. Wahl 박사
"특화된 세포를 한동안 재프로그래밍할 수 있었지만 신체에서 자발적으로 발생하는 것을 방지하는 제어 메커니즘과 페트리 접시에서 운명을 바꾸는 것이 왜 그렇게 어려운지에 대해서는 알려진 바가 없었습니다." 말한다 후안-카를로스 이즈피수아 벨몬테, Ph.D., 유전자 발현 연구실 교수, 제프리 M. 월, Ph.D., 유전자 발현 연구실의 교수이기도 합니다.
그들의 발견은 iPSCs 기술이 환자별 줄기 세포의 공급원으로서의 약속을 이행하는 데 한 걸음 더 다가갔지만 과학자들이 암 발병을 재고하도록 강요했습니다.
Wahl은 "완전히 헌신하고 전문화된 세포의 탈분화를 통해 암이 발생한다는 53년 된 생각이 있었지만 결국 현재 유행하는 암 줄기 세포 이론에 찬성하여 폐기되었습니다."라고 말합니다. "이제 우리는 p53이 역분화를 막는다는 사실을 알았으므로 거의 모든 암세포가 어떤 식으로든 pXNUMX 기능을 잃기 때문에 리프로그래밍이 암 발병에 역할을 할 가능성을 재고해야 할 때라고 생각합니다."
포유류 배아가 일련의 발달 단계를 거치면서 거의 무한한 전망을 즐기는 배아 줄기 세포의 선택은 점진적으로 제한되어 마침내 우리 몸을 구성하고 일반적으로 되돌릴 수 있는 능력이 부족한 약 200개의 세포 유형을 생성하게 됩니다. 덜 전문화 된 단계로 돌아갑니다.
분화는 일반적으로 돌이킬 수 없지만, 과학자들은 재프로그래밍되는 것을 꺼리는 세포를 극복하기 위해 몇 가지 방법을 개발했습니다. 가장 널리 사용되는 기술은 4가지 전사 인자(Oct2, Sox4, KlfXNUMX 및 c-Myc-in 완전 커밋된 성인 세포)의 강제 발현을 포함합니다.
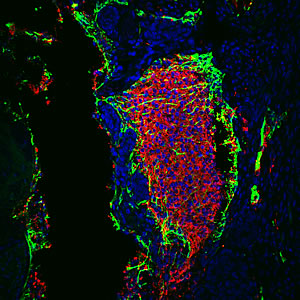
p53 활동을 하향 조절하면 일반적인 XNUMX개 대신 XNUMX개의 리프로그래밍 인자만 필요한 성인 체세포의 리프로그래밍 효율이 증가합니다.
이미지: Salk Institute for Biological Studies, Dr. Juan-Carlos Belmonte 제공
"안타깝게도 Klf4와 c-Myc는 발암 유전자이며 이들을 추가하면 암을 유발할 위험이 있습니다."라고 Belmonte는 말합니다. 그러나 이러한 강력한 발암유전자가 제공하는 추가적인 압박에도 불구하고 아주 작은 부분만이 배아 줄기 세포처럼 보이고 행동하는 iPSC로 변형되어 Belmonte는 세포를 재프로그래밍하기 위해 무엇을 했는지에 대해 의문을 제기했습니다. 성장에서?
옆집 이웃인 암 전문가 Wahl과의 대화에서 실험실에서 테스트할 수 있는 몇 가지 신선한 아이디어를 제공했습니다. "일반적으로 세포는 재프로그래밍되지 않으므로 이를 방지하는 메커니즘이 있어야 합니다."라고 Wahl은 말합니다. "우리는 c-Myc와 재프로그래밍에 필요한 다른 유전자 중 일부가 종양 억제 인자 p53을 활성화한다는 것을 알고 있었고 그것이 어떤 역할을 하는지 궁금했습니다."
물론 박사후 연구원 및 공동 제4저자인 Teruhisa Kawamura 박사와 Jotaro Suzuki 박사의 실험에서 c-Myc 및 Klf53 재프로그래밍 인자를 단독으로 또는 다양한 조합으로 추가하면 p53이 활성화된다는 사실이 밝혀졌습니다. 좁은 길. 첫 번째 응답자로서 종양 억제 인자 p53은 세포가 스트레스 조건을 경험할 때 작동하도록 호출됩니다. 상황에 따라 pXNUMX은 수리할 시간을 허용하기 위해 세포 분열을 중단하는 유전자를 활성화하거나, 모든 구조 시도가 무익한 것으로 판명되면 세포 분열을 영원히 중단하거나 자살하도록 명령합니다.
p53이 결핍되도록 유전자 조작된 세포에서 재프로그래밍 효율은 대조군 세포에 비해 최소 10배 증가했으며, 이는 p53이 줄기와 같은 상태로 되돌리려는 세포를 지배하는 데 중요한 역할을 한다는 것을 분명히 보여줍니다.
리프로그래밍 인자의 완전한 보완으로 생성된 iPSC는 악성으로 변할 위험이 있기 때문에 Belmonte와 그의 팀은 p53이 결여된 마우스 세포가 Oct4와 Sox2라는 두 가지 인자만 사용하여 리프로그래밍할 수 있는지 여부를 알고 싶었습니다. 세포는 쉽게 iPSC로 전환되었고 만능 배아 줄기 세포에 대한 궁극적인 테스트를 통과하여 번식할 수 있는 건강한 만삭 쥐를 낳았습니다.
"이 매우 성공적인 협업은 Salk를 특별한 장소로 만드는 주요한 예입니다."라고 Wahl은 말합니다. “Juan Carlos와 저는 매일 대화를 나누며 매우 다른 관점에서 같은 질문에 접근합니다. 그는 발달 생물학의 관점에서 왔고, 나는 암의 관점에서 왔지만 함께 모이면 훌륭한 이야기를 만들 수 있습니다.”
이 기술의 상용화에 대한 정보는 (858) 453-4100, Ext. 1278.
이 작업은 National Institutes of Health, Tercel, Marato, G. Harold 및 Leila Y. Mathers Charitable Foundation 및 Fundacion Cellex의 보조금에 의해 지원되었습니다.
이 작업에 기여한 연구원으로는 Yunyuan V. Wang, Ph.D. Wahl 연구소, Sergio Menendez, Ph.D., Laura Batlle Morera, Ph.D., Angel Raya, Ph.D., 모두 스페인 바르셀로나의 재생 의학 센터에 있습니다.
Salk Institute of Biological Studies 정보 :
Salk Institute for Biological Studies는 세계적으로 유명한 기초 연구 기관 중 하나로, 국제적으로 유명한 교수진이 독특하고 협력적이며 창의적인 환경에서 근본적인 생명 과학 문제를 조사합니다. 미래 세대의 연구원을 발견하고 멘토링하는 데 중점을 둔 Salk 과학자는 신경 과학, 유전학, 세포 및 식물 생물학 및 관련 분야를 연구하여 암, 노화, 알츠하이머, 당뇨병 및 심혈관 질환에 대한 이해에 획기적인 기여를 합니다.
교수진의 업적은 노벨상 및 국립 과학 아카데미 회원을 포함하여 수많은 영예로 인정되었습니다. 1960년 소아마비 백신 개척자인 Jonas Salk, MD가 설립한 이 연구소는 독립적인 비영리 조직이자 건축학적 랜드마크입니다.
커뮤니케이션 사무소
전화 : (858) 453-4100
press@salk.edu