
2025 년 5 월 23 일
Salk 연구소와 UC San Diego 연구원들은 다이네인-Lis1 단백질 상호작용에 대한 최초의 영상을 포착하여 신경 질환에 대한 미래 약물 개발을 지원합니다.
Salk 연구소와 UC San Diego 연구원들은 다이네인-Lis1 단백질 상호작용에 대한 최초의 영상을 포착하여 신경 질환에 대한 미래 약물 개발을 지원합니다.
LA JOLLA—우리 세포는 미세한 고속도로와 특수 단백질 운반체에 의존하여 이동합니다. 모두-세포 소기관의 위치를 정하는 것부터 단백질 지시를 전달하는 것, 그리고 세포 쓰레기를 처리하는 것까지. 이러한 고속도로(미세소관)와 운반체(운동 단백질)는 세포 기능과 생존에 필수적입니다.

운동 단백질과 관련 단백질의 기능 장애는 심각한 신경발달 및 신경퇴행성 질환으로 이어질 수 있습니다. 예를 들어, 운동 단백질 다이네인의 파트너 단백질인 Lis1의 기능 장애는 드물지만 치명적인 선천적 기형인 뇌수종(lissencephaly), 즉 "평활뇌"를 유발할 수 있으며, 이 질환에 대한 치료법은 아직 없습니다. 그러나 다이네인이나 Lis1 기능을 표적으로 삼아 회복시키는 치료법은 이러한 암울한 결과를 바꿀 수 있으며, 이러한 치료법의 개발은 다이네인과 Lis1의 상호작용을 철저히 이해하는 데 달려 있습니다.
솔크 연구소와 UC 샌디에이고의 새로운 연구는 Lis1이 다이네인을 "활성화"하는 모습을 담은 단편 영상을 촬영했습니다. 이 영상을 통해 연구팀은 두 단백질이 상호작용할 때 나타나는 16가지 형태를 분류할 수 있었는데, 그중 일부는 이전에는 관찰되지 않았습니다. 이러한 통찰력은 약물이 단백질과 상호작용할 수 있는 정확한 위치를 밝혀내므로, 다이네인과 Lis1의 기능을 회복하는 미래 치료제 개발의 기반이 될 것입니다.
연구 결과는 자연 구조 및 분자 생물학 5 월 23, 2025.
“저는 항상 모터 단백질에 관심이 있었지만 다이네인은 세포 중심을 향해 이동할 수 있는 유일한 모터 단백질이기 때문에 저에게 특히 매력적입니다.”라고 공동 저자가 말했습니다. 아그네츠카 켄드릭솔크 대학교 조교수인 그는 "오늘날 우리 연구실에 있는 인상적인 도구들을 통해 다이네인과 리스1의 실시간 상호작용 영상을 제작할 수 있었습니다. 이들의 단계적 협력 관계를 자세히 살펴보면 신경발달 및 신경퇴행성 질환에서 이들의 활성을 회복하는 방법을 찾는 데 도움이 될 것입니다."라고 말했습니다.
배경: 다이네인 잠금 해제
다이네인은 두 개의 동일한 반쪽으로 구성되어 있으며, 각 반쪽은 1) 미세소관에 부착되는 "줄기", 2) 단백질이 끌어당기는 물질에 부착되는 "꼬리", 그리고 3) 이동에 동력을 제공하는 "모터"를 포함합니다. 다이네인의 물리적 움직임은 걷는 것과 비슷합니다. 모터가 ATP라는 세포 연료를 소모함에 따라, 줄기는 교대로 분리되었다가 앞으로 휘둘러졌다가 아래쪽 미세소관에 다시 부착됩니다.
다이네인은 귀중한 유전자 저장고인 핵으로 향하는 일방통행 티켓이기 때문에 그 활동은 엄격하게 조절됩니다. 다이네인이 아무것도 운반하지 않을 때는 미세소관 고속도로에서 완전히 분리되어 "파이(Phi)"라고 불리는 잠긴 상태로 자유롭게 떠다닙니다. 지난 몇 년 동안 켄드릭과 동료들은 다이네인이 어떻게 "잠금 해제"되는지를 규명하기 위해 열심히 연구해 왔습니다.
지금까지 그들의 연구는 Lis1이 다이네인 구조에 쐐기처럼 끼어들어 "Chi"라는 열린 형태로 풀어주는 열쇠 역할을 한다는 것을 밝혀냈습니다. 그러나 이러한 통찰은 다이네인과 Lis1의 상호작용의 다양한 단계에 걸쳐 산발적으로 촬영한 정지 영상에 기반했습니다. 이러한 정지 영상에서 배울 점은 많았지만, 두 단백질이 어떻게 상호작용하는지에 대한 더 깊은 이해는 실제로 작용하는 모습을 관찰해야만 얻을 수 있었습니다.
주요 발견: Lis1과 다이네인의 상호 작용
"다이네인과 Lis1을 영상화하는 저희의 접근법은 이 단백질에 대한 이전 연구보다 훨씬 포괄적입니다."라고 공동 교신저자인 UC 샌디에이고의 안드레스 레슈지너 교수는 말했습니다. "사진이 아닌 영상을 촬영함으로써, 다이네인이 Lis16과 상호작용할 때 나타나는 3가지의 상세한 1차원 형태를 확인했습니다. 그중 몇몇은 저희 연구에서만 발견할 수 있는 독특한 형태입니다."
연구팀은 효모 모델을 사용하여 다이네인과 Lis1을 포착했습니다. 인간 세포와 달리 효모 세포는 다이네인과 Lis1 수치가 변화해도 생존할 수 있기 때문입니다. 또한 다이네인의 구조가 인간 세포와 효모 세포 모두에서 기능적으로 동일하기 때문에, 효모 다이네인에 대해 알아낸 내용을 인간 다이네인에도 적용할 수 있습니다.
이 효모 모델을 이용하여 연구진은 다이네인과 Lis1을 분리하고 온도를 극적으로 낮춰 다이네인의 활성을 늦췄습니다. 그런 다음, 시간 분해능 극저온 전자 현미경(cryo-EM)을 이용하여 다이네인과 Lis3의 상호작용을 고해상도 1D 영상으로 포착했습니다. 이 영상은 다이네인의 파이(Phi, 잠금) 상태와 카이(Chi, 잠금 해제) 상태 사이의 타임라인을 나타낼 수 있습니다.
Cryo-EM은 전자빔을 사용하여 원자 단위까지 세부적으로 표현된 분자의 3D 영상을 구축합니다. 이전 연구에서는 Cryo-EM 및 기타 이미징 방법을 사용하여 다이네인의 잠금 상태와 잠금 해제 상태의 영상을 구축했습니다. 시간 해결 하지만 이 구성 요소는 새로운 것입니다. 단일 시점에 단일 구조를 포착하는 대신, 시간 분해능 포착은 시간 경과에 따라 다양한 구조를 식별하여 영상을 생성합니다. 이를 통해 솔크와 UC 샌디에이고 과학자들은 다이네인 구조의 1초 미만 단위 변화를 추적하여 잠금 상태에서 잠금 해제 상태로 전환되는 데 필요한 단계별 과정을 설명할 수 있었습니다.
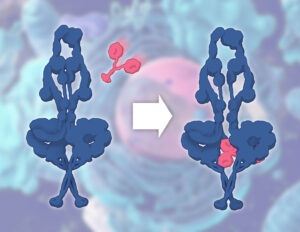
새로운 영상은 다이네인을 활성화하는 첫 번째 단계가 Lis1이 다이네인의 모터 소단위체에 부착되는 것을 보여줍니다. 다이네인과 마찬가지로 Lis1도 두 개의 동일한 반쪽으로 이루어져 있습니다. 이 첫 번째 상호작용에서 Lis1의 한쪽 반쪽이 다이네인에 부착되어 다이네인의 고정 상태를 해제하고, 모양을 변화시켜 모터를 작동시켜 자연의 에너지 분자인 ATP를 더욱 빠르고 효율적으로 활용합니다. ATP를 연료로 하는 이 엔진을 작동시키는 것은 다이네인이 세포의 미세소관 고속도로를 따라 이동하는 능력을 시작하는 데 핵심적입니다.
그런 다음 Lis1의 두 번째 절반이 다이네인에 부착되는데, 이번에는 줄기에 부착됩니다. 이 두 번째 Lis1 상호작용은 활성화를 완료하고 다이네인의 기(Chi) 상태를 강화합니다. 또한 다이네인의 운동 활성을 더욱 증가시켜 활동을 촉진합니다.
미래 전망: 발달 및 신경 장애에서 Lis1 및 다이네인 기능 장애 복구
켄드릭은 "이러한 연구 결과는 Lis1 기능 장애가 다이네인 활동에 그토록 파괴적인 영향을 미치는 이유와 그것이 향후 발달 및 신경 장애에 어떻게 영향을 미치는지 이해하는 데 그 어느 때보다 가까이 다가가는 계기가 되었습니다."라고 말했습니다.
다이네인과 Lis3에 대한 새로운 고해상도 1D 구조적 통찰력은 신경발달 및 신경퇴행성 질환에서 이들의 기능 장애를 치료하는 길을 열어줄 수 있습니다. 향후 연구를 통해 Lis1의 다양한 돌연변이가 다이네인과의 상호작용에 어떤 영향을 미치는지, 그리고 이것이 뇌수막염 및 기타 희귀 유전 질환에 어떻게 기여하는지 탐구할 수 있습니다. 궁극적으로 이 두 단백질의 물리적 구조에 대한 지식이 더 많아질수록, 해당 구조에 "적합"하고 활성을 회복시키는 약물을 개발하는 것이 더 쉬워질 것입니다.
이 논문에 대한 추가 정보
다른 저자로는 UC San Diego의 Kendrick Nguyen, Eva Karasmanis 및 Rommie Amaro가 있습니다. UC San Diego의 Samara Reck-Peterson 및 Howard Hughes Medical Institute; 그리고 버몬트 대학의 Wen Ma.
이 연구는 미국 암 협회(PF-18-190-01-CCG), 국립 보건원(P30 CA014195, T32 GM139795, R01 GM107214, R35 GM145296, R35 GM141825), 버몬트 심혈관 연구소, 제인 코핀 차일즈 박사후 연구원, 하워드 휴즈 의학 연구소의 지원을 받았습니다.
DOI : 10.1038 / s41594-025-01558-w
일지
자연 구조 및 분자 생물학
작가
Agnieszka A. Kendrick, Kendrick HV Nguyen, Wen Ma, Eva P. Karasmanis, Rommie E. Amaro, Samara L. Reck-Peterson 및 Andres E. Leschziner
커뮤니케이션 사무소
전화 : (858) 453-4100
press@salk.edu
솔크 연구소는 최초의 안전하고 효과적인 소아마비 백신 개발자인 조너스 솔크가 1960년에 설립한 독립적인 비영리 연구 기관입니다. 연구소의 사명은 암, 알츠하이머병, 농업 취약성 등 사회가 직면한 가장 시급한 문제들을 해결하기 위한 기초적이고 협력적이며 과감한 연구를 추진하는 것입니다. 이러한 기초 과학은 모든 응용 연구의 기반이 되어 전 세계적으로 새로운 의약품과 혁신을 가능하게 하는 통찰력을 제공합니다.