Amerikanische Krebsgesellschaft Professor
Labor für Molekular- und Zellbiologie
Renato-Dulbecco-Stiftungsprofessur


Zellen sind wie Gewohnheitstiere – sie durchlaufen immer wieder denselben Zellzyklus und koordinieren dabei die Aktivierung von Genen und Proteinen mit Wachstum und Teilung. Wenn dieser Zyklus gestört wird, gerät alles aus den Fugen: Zellen beginnen, die falschen Gene zu kopieren, Proteine zur falschen Zeit zu aktivieren oder sich zu schnell oder zu langsam zu teilen. All diese Störungen können zu Krebs führen. Das Verständnis, wie eine gesunde Zelle ihren Wachstumszyklus steuert, kann Forschern helfen, besser zu verstehen, was in Tumorzellen schiefgeht, wenn ihr Wachstum außer Kontrolle gerät – und wie man es beheben kann. Es ist jedoch schwierig, genau zu bestimmen, welche einzelnen Gene und Proteine am wichtigsten sind.
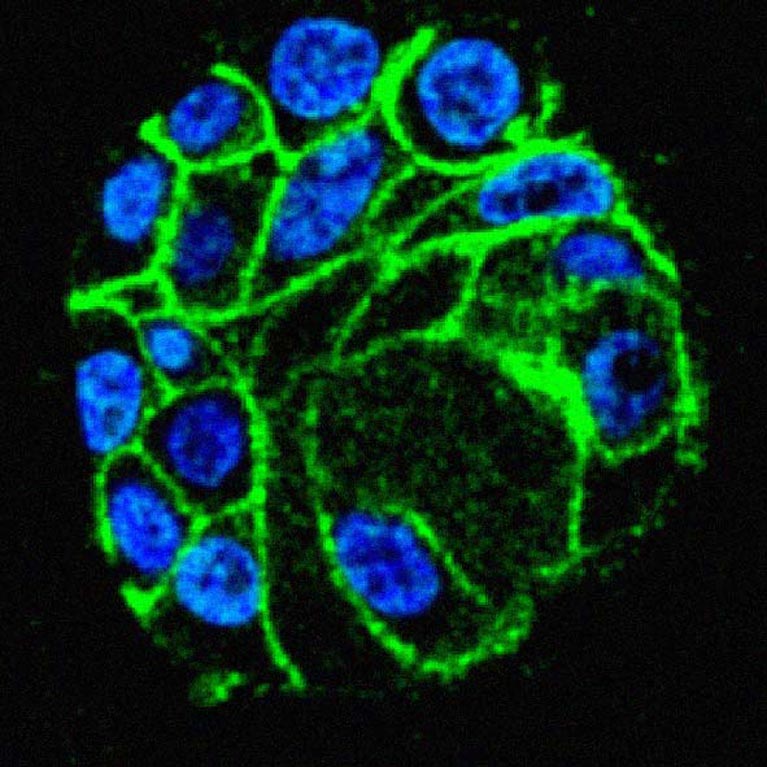
Tony Hunter machte vor über vier Jahrzehnten die bahnbrechende Entdeckung, dass die Zugabe und Abspaltung von Phosphatmolekülen zu Proteinen auf Tyrosin, einer der 20 Aminosäuren, es den Zellen ermöglicht zu steuern, wann wichtige Proteine im Bereitschafts- und wann sie im aktiven Zustand sind. Er zeigte dann, dass bei Krebs das Wachstum durch Fehlfunktionen dieser Phosphate in einen ständigen Aktivierungsmodus umgeschaltet wurde. Seitdem hat sein Labor die Forschung in der Erkenntnis vorangetrieben, wie chemische Modifikationen von Proteinen den Zellzyklus und das Wachstum steuern. Hunter nutzt modernste molekulare, genetische und zellbiologische Techniken, um zu untersuchen, wie diese Programme miteinander interagieren, welche Auswirkungen sie auf Zellen haben und wie Krebs sie stört, um ungehemmtes Wachstum zu fördern.
Bereits heute wurden Krebsmedikamente – wie die Leukämie-Therapie Gleevec™ – auf der Grundlage von Hunters Entdeckungen entwickelt. Gleevec schaltet ein Enzym aus, das normalerweise Phosphatgruppen an Tyrosine in Proteinen anfügt, und verhindert so das Wachstum von Krebs. Während Hunter weiterhin andere Wege entdeckt, wie Zellen chemische Zusätze zu Proteinen nutzen, um ihr Wachstum zu steuern, zielt er darauf ab, potenzielle therapeutische Angriffspunkte für Krebs zu finden.
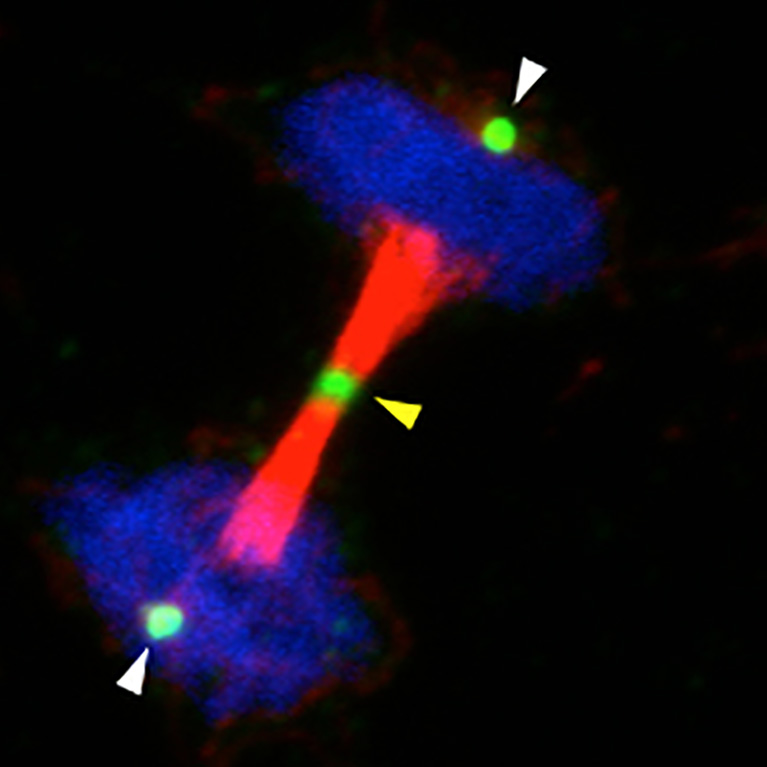
Hunter zeigte, dass ein Mechanismus namens Tyrosinphosphorylierung (die Anlagerung von Phosphatmolekülen an eine Aminosäure in Proteinen) als zentraler Schalter für eine Reihe von Schlüsselproteinen fungiert. Diese Entdeckung hat zu neuen, erfolgreichen Krebstherapien geführt.
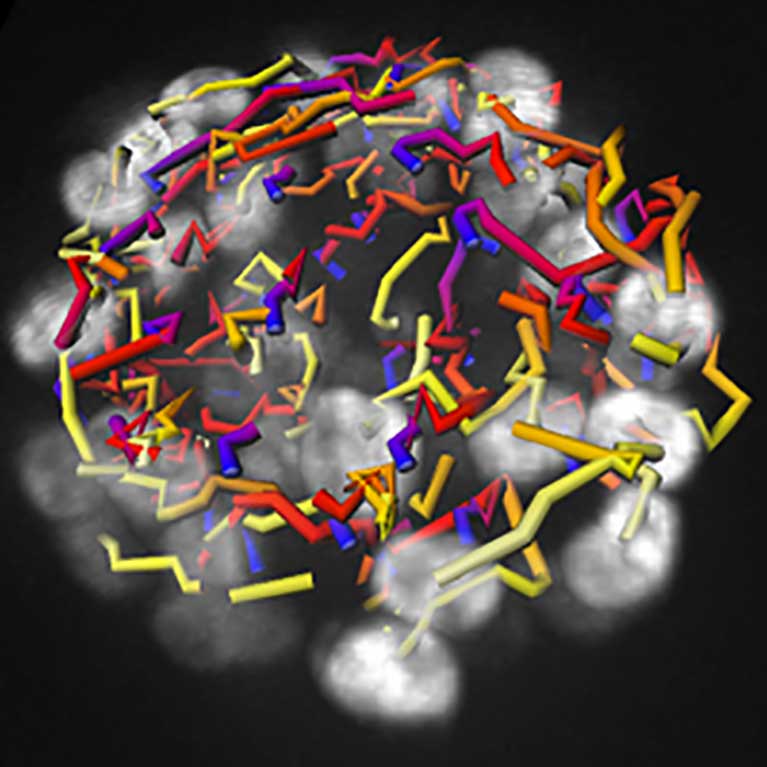
Hunter half zu erklären, wie genau Zellen ihre Reparatur-Teams mobilisieren, um beschädigte DNA zu reparieren, ein wichtiger Mechanismus zur Verhinderung von Krebsentstehung.
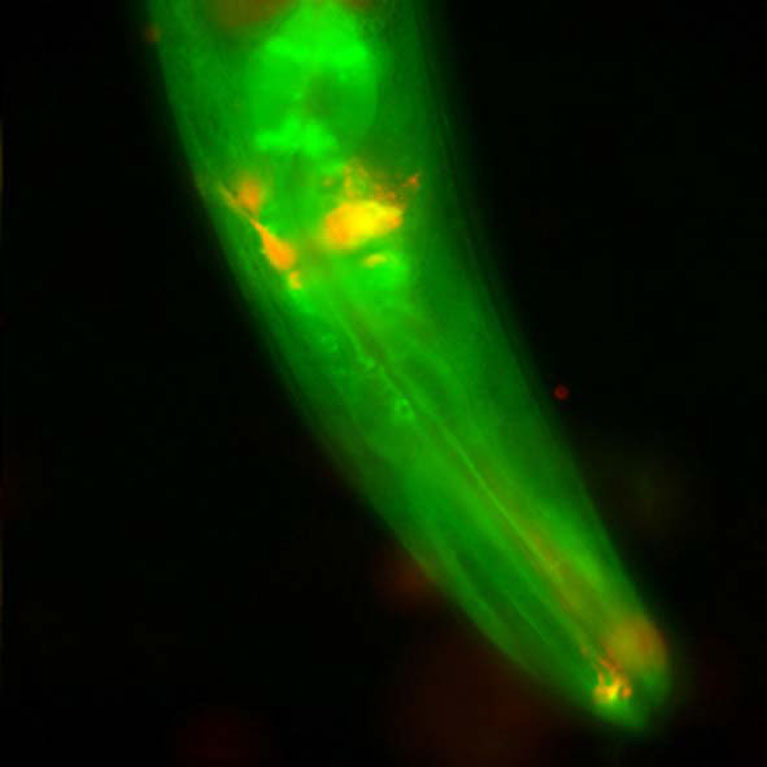
Hunter zeigte, wie einige Krebsarten eine Lücke im zellulären Sicherheitssystem finden, das sie eigentlich zerstören sollte, was ihnen hilft, sich nach der Behandlung mit DNA-schädigenden Krebsmedikamenten zu erholen und weiter zu teilen. Bei Bauchspeicheldrüsenkrebs können Medikamente den Tumor aufgrund einer entzündlichen Barriere, die durch die Wechselwirkung zwischen dem Tumor und den Bauchspeicheldrüsenzellen entsteht, nicht erreichen. Hunter hat jedoch einen Weg gefunden, diese Kommunikation über ein Signalmolekül namens LIF zu stören. LIF könnte ein nützlicher Biomarker oder ein Ziel für die Behandlung von Bauchspeicheldrüsenkrebs sein.
BA, Auszeichnung erster Klasse, Universität Cambridge, England
Promotion, Universität Cambridge, England
Postdoc, Salk Institute und University of Cambridge