
24. April 2012
Salk-Wissenschaftler haben herausgefunden, dass ein lange übersehenes Protein das Tor zur Speicherung und Verbrennung von Fett sein könnte
Salk-Wissenschaftler haben herausgefunden, dass ein lange übersehenes Protein das Tor zur Speicherung und Verbrennung von Fett sein könnte
LA JOLLA, Kalifornien – Der Mensch ist darauf ausgelegt, nach Fett zu hungern, es während der Festzeiten anzuhäufen und in Zeiten der Hungersnot zu verbrennen. Wenn der moderne Taillenumfang jedoch mit fett- und zuckerreichen Lebensmitteln überschwemmt wird, übersteigt er oft bei weitem den Bedarf, Energie für magere Zeiten zu speichern, und die Folge ist eine Epidemie von Diabetes, Herzerkrankungen und anderen Problemen im Zusammenhang mit Fettleibigkeit.
Jetzt haben Wissenschaftler am Salk Institute for Biological Studies den Dreh- und Angelpunkt des Fettstoffwechsels identifiziert, ein Protein namens Fibroblasten-Wachstumsfaktor 1 (FGF1), das neue Wege bei der Behandlung von Diabetes eröffnen könnte.
In einem am 22. April veröffentlichten Artikel NaturDas Evans-Labor berichtet, dass die FGF1-Aktivität durch eine fettreiche Ernährung ausgelöst wird und dass sich Mäuse, denen das Protein fehlt, schnell entwickeln Diabetes. Dies deutet darauf hin, dass FGF1 für die Aufrechterhaltung der Insulinempfindlichkeit des Körpers und eines normalen Blutzuckerspiegels von entscheidender Bedeutung ist.
„Weil Menschen in Zeiten des Überflusses gut darin sind, Fett zu speichern, sind wir auch hervorragend darin, Zeiten einer Hungersnot zu überleben“, sagt er Ronald M. Evans, ein Professor in Salk's Genexpressionslabor und Hauptautor des Artikels. „Das Fettgewebe unseres Körpers ist wie eine Batterie, die uns bei Nahrungsknappheit mit einer stetigen Energiequelle versorgt. FGF1 steuert die Ausdehnung und Kontraktion von Fett und steuert so das Auf und Ab der Energie in unserem Körper.“

Ron Evans, Professor Gene Expression Laboratory, Michael Downes, leitender Wissenschaftler und Jae Myoung Suh, Postdoktorand.
Bild: Mit freundlicher Genehmigung des Salk Institute for Biological Studies
Die Fettleibigkeitsrate ist in den Vereinigten Staaten in den letzten Jahrzehnten sprunghaft angestiegen, wobei mehr als ein Drittel der US-Erwachsenen und 17 Prozent der Kinder und Jugendlichen mittlerweile als fettleibig gelten, heißt es in der Studie Centers for Disease Control and Prevention.
Da die Zahl der übergewichtigen Menschen zunimmt, steigt auch die Häufigkeit von Stoffwechselerkrankungen. Schätzungen zufolge leiden fast 26 Millionen Amerikaner an Typ-2-Diabetes im Zusammenhang mit Fettleibigkeit. Mit jährlichen Kosten von weit über 200 Milliarden US-Dollar ist Fettleibigkeit eine chronische Krankheit, die einen großen Teil unserer Gesundheitsausgaben verschlingt.
Obwohl Bewegung und Kalorieneinschränkung bekanntermaßen wirksam bei der Vorbeugung und Behandlung von Diabetes sind, nimmt die Fettleibigkeitsepidemie weiter zu und neue Medikamente zur Behandlung des Problems werden dringend benötigt. Vor diesem Hintergrund ist die Entdeckung im Evans-Labor ein wichtiger Durchbruch – und eine Überraschung.
„Die Entdeckung von FGF1 war unerwartet – und faszinierend –, weil angenommen wurde, dass es nichts bewirkt“, sagt Jae Myoung Suh, Postdoktorand in Evans‘ Labor und Co-Erstautor der Arbeit. „Wenn man dem Körper FGF1 entzieht, passiert nichts, wenn die Mäuse regelmäßig eine fettarme Diät erhalten. Bei einer fettreichen „westlichen“ Ernährung entwickeln die Mäuse jedoch eine aggressive Form von Diabetes und erleben einen systemweiten Zusammenbruch ihrer Stoffwechselgesundheit.
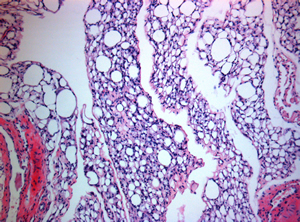
Die Salk-Forscher entdeckten, dass Mäuse, denen ein Protein namens Fibroblasten-Wachstumsfaktor 1 (FGF1) fehlte, nicht in der Lage waren, Fett normal zu speichern und zu nutzen.
Als diese Mäuse von einer fettreichen Ernährung auf eine normale Ernährung umgestellt wurden, entwickelten sie ungleichmäßige Fettklumpen (im Bild oben weiß dargestellt) in ihrem Körpergewebe, was darauf hindeutet, dass ihre Fettstoffwechselmechanismen schief gelaufen waren.
Bild: Mit freundlicher Genehmigung von Jae Myoung Suh, wissenschaftlicher Mitarbeiter, Gene Expression Laboratory
„Diese Anomalien führen zu einer Entzündung des Bauch- oder Magenfetts“, sagt Michael Downes, leitender Wissenschaftler im Gene Expression Laboratory von Salk und Co-Hauptautor der Studie. „Dies ist wichtig, da entzündetes viszerales Fett mit einem erhöhten Risiko für Diabetes und andere mit Fettleibigkeit verbundene Krankheiten wie Herzerkrankungen und Schlaganfall in Verbindung gebracht wird.“
Die Wissenschaftler fanden außerdem heraus, dass FGF1 durch das Antidiabetikum Actos reguliert wird, das zur Erhöhung der Insulinempfindlichkeit des Körpers eingesetzt wird. Aber Actos und verwandte Medikamente sind zwar hilfreich, haben aber Nebenwirkungen, die ihren Einsatz einschränken.
Daher planen Evans und seine Kollegen zu untersuchen, ob FGF1 einen neuen Weg zur Diabeteskontrolle aufzeigen könnte, indem die Nachteile von Actos vermieden und ein natürlicheres Mittel zur Erhöhung der Insulinsensitivität bereitgestellt werden.
Johan Jonker, ein ehemaliger Postdoktorand in Evans‘ Labor, jetzt an der Universität Groningen, Niederlande, war Co-Erstautor des Artikels. Weitere Autoren des Artikels waren: Annette Atkins, Maryam Ahmadian, Jamie Whyte, Mingxiao He, Henry Juguilon, Yun-Qiang Yin, Colin Phillips und Ruth Yu vom Salk Institute; und Pingping Li, Jerrold Olefsky und Robert Henry von der University of California, San Diego.
Die Forschung wurde von den National Institutes of Health, dem Leona M. and Harry B. Helmsley Charitable Trust und dem Howard Hughes Medical Institute unterstützt.
Über das Salk Institute for Biological Studies:
Das Salk Institute for Biological Studies ist eine der weltweit herausragenden Grundlagenforschungseinrichtungen, in der international renommierte Dozenten in einem einzigartigen, kollaborativen und kreativen Umfeld grundlegende Fragen der Biowissenschaften untersuchen. Salk-Wissenschaftler konzentrieren sich sowohl auf Entdeckungen als auch auf die Betreuung zukünftiger Forschergenerationen und leisten bahnbrechende Beiträge zu unserem Verständnis von Krebs, Alterung, Alzheimer, Diabetes und Infektionskrankheiten, indem sie Neurowissenschaften, Genetik, Zell- und Pflanzenbiologie und verwandte Disziplinen studieren.
Die Leistungen der Fakultät wurden mit zahlreichen Ehrungen gewürdigt, darunter Nobelpreise und Mitgliedschaften in der National Academy of Sciences. Das 1960 vom Polioimpfpionier Jonas Salk, MD, gegründete Institut ist eine unabhängige gemeinnützige Organisation und ein architektonisches Wahrzeichen.
JOURNAL
Natur
TITEL
Eine PPARγ-FGF1-Achse ist für den adaptiven Fettumbau und die metabolische Homöostase erforderlich
AUTOREN
Johan W. Jonker, Jae Myoung Suh, Annette R. Atkins, Maryam Ahmadian, Pingping Li, Jamie Whyte, Mingxiao He, Henry Juguilon, Yun-Qiang Yin, Colin T. Phillips, Ruth T. Yu, Jerrold M. Olefsky, Robert R. Henry, Michael Downes und Ronald M. Evans
Büro für Kommunikation
Tel: (858) 453-4100
press@salk.edu